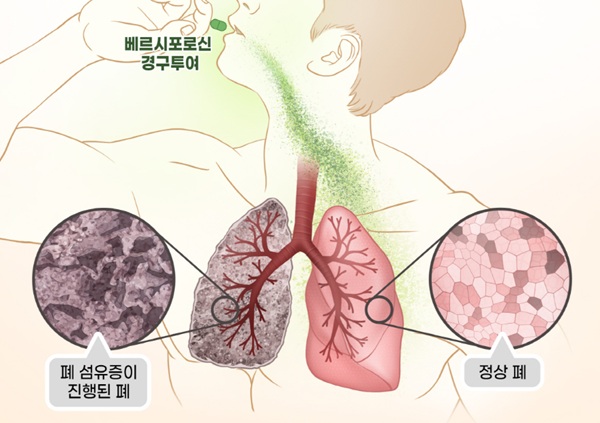
대웅제약이 특발성 폐섬유증(IPF) 치료제로 개발 중인 ‘베르시포로신(코드명 DWN12088)’의 임상 2상 환자 모집 마무리 작업을 진행 중이다.
대웅제약은 임상 환자 모집을 3월 말까지 마치고 2027년 1분기까지 임상 2a상 데이터를 확보할 계획이었는데 환자 모집이 아직 완료되지 않은 것으로 확인됐다.
회사가 제시한 목표치를 맞추지 못하면 파이프라인의 기술수출에 있어서 개발 실행력 지표가 낮게 평가받는 등 가치 하락 문제가 생길 수 있고 개발 역량에 대한 의문을 불러일으킬 수 있다.
대웅제약 관계자는 “베르시포로신 임상 환자 등록 등 과정을 차질 없이 진행 중”이라고 말했다.
대웅제약이 한국과 미국에서 임상 2상을 진행 중인 베르시포로신을 내년 1분기까지 소규모 환자 대상 약효 확인(2a상)을 마친 후 투약 조건 최적화(2b상)에 나설 계획이다.
IPF는 폐가 딱딱하게 굳으면서 기능을 상실(섬유화)하는 질병이다. PRS는 콜라겐의 주요 구성 성분인 프롤린을 활성화해 콜라겐 생합성에 관여하는 효소다. 과도한 콜라겐 생성은 폐 섬유화의 원인이 된다. 이 질병은 진단 이후 5년 내 생존율이 45.6% 미만인 것으로 알려져 있다.
대웅제약은 베르시포로신을 세계 첫 PRS(Prolyl-tRNA Synthetase) 선택적 억제 기전 경구용 항섬유화제로 개발하고 있다.
선택적으로 억제한다는 건 해당 원인에만 작용해 타 부위의 이상반응 부담은 줄여주고 효과는 높인다는 뜻이다. 인체에서 콜라겐 부족은 심혈관 질환 등 각종 질병 및 사망의 원인이 되는데, 베르시포로신의 경우 PRS만 타깃해 부작용 위험성을 줄이도록 설계됐다.
베르시포로신은 임상 1상에서 위약군 대비 제3형 프로콜라겐 펩타이드(Pro-C3) 수치가 낮은 것으로 나타났다. Pro-C3은 콜라겐이 새로 만들어지면서 나오는 물질로 혈중 수치가 낮다는 건 비교적 섬유화 활동이 억제된 것으로 해석할 수 있다.
베르시포로신은 안전성 측면에서도 경쟁력을 가질 수 있을 것으로 전망된다. 섬유화 속도를 늦추는 기존 치료제는 장기 복용이 불가피한데 임상에서 설사 등 위장관 부작용으로 투약이 중단되는 사례가 있었다.
베르시포로신은 임상 1상에서 투약을 중단할 정도의 중대한 이상반응이 나타나지 않았다. 설사, 구토 등 위장관계 부작용이 있었으나 이를 보완하고자 용액 제형에서 장용정으로 제형을 변경해 1상을 마쳤다.
2022년 6월부터 진행 중인 글로벌 임상 2상에서도 독립적 데이터 모니터링 위원회(IDMC)로부터 두 차례에 걸쳐 임상 지속 권고를 받았다. 해당 위원회는 미국 식품의약국(FDA) 산하에서 개별 임상시험의 안전성, 지속 여부 등을 검토하기 위해 외부 전문가들로 구성된다.
향후 과제는 임상 2상에서의 효능 입증이다. 2023년 1월 영국 CS파마슈티컬스와 베르시포로신 중국 상업화를 내용으로 3억3600만 달러(한화 약 4130억 원) 규모기술수출 계약을 체결했는데 2025년 3월 파트너사 전략 변경에 따라 반환됐다. 임상 2상 데이터를 통해 파이프라인 가치를 높일 필요가 있다는 지적이 나오는 이유다.
[소비자가만드는신문=정현철 기자]



